Кетони - химическа енциклопедия
Кетони. карбонил порт. в-която група С = О е свързан с два въглеродни атома Съгласно номенклатурата на IUPAC. заглавия. кетони, образувани от присъединяването позоваванията. съответния въглеводород суфикса "то" или заглавия. радикали, свързани с кето група С = О, думите "кетон"; в присъствието на по-стар кето група означена с префикс "оксо". Напр. Кон. СН3 СН 2 СН 2 СН 3 SOSN2 наречен. 3-хексанон или etilpropilketon, съед. СН3 СН2 СООН SOSN2 - 4-оксопентанова-та. За някои кетони приема тривиални препратки. (Вж. Таблица.).
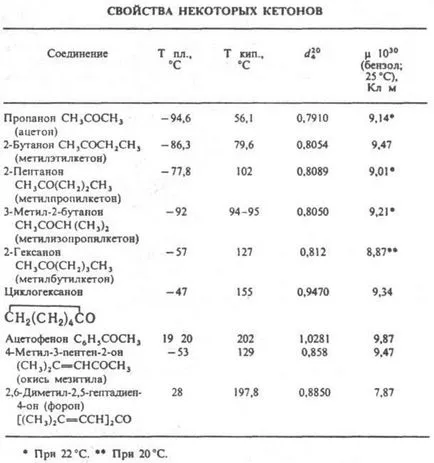
Особен клас от циклични. ненаситени. дикетони - хинони.
спектрите IR на характеристика кетон. абсорбционни ивици на разтягане вибрации на С = О групи лежат в честотния обхват (Vc = О) 1720-1700 cm -1 (alifatich. кетони) 1820-1700sm -1 (циклични кетони.), и Vc = O нараства с увеличаване на напрежението цикъл. При сдвояването на С = О групи с множество връзки, или арил Vc = О се намалява с 20-40 cm -1. Chem. протон смени -metilenovyh кетонни групи в спектрите PMR са в област 2-3 ррт и метиленовата група в близост до двата карбонила (за дикетони), - в ррт област 3-4;.. Chem. 13 смени групата С = О в 13С NMR спектрите са в диапазона от 200-220 ррт Електронни кетони спектри съдържат типични ленти с л макс 270-300 нм (например 15-20), съответстваща на стр. P възел. За конюгиран моно-, ди- и полиенов кетони Naib. характерни абсорбционни ивици при р. р * - преходи, L макс 200-300 нм (е 10,000 и по-горе). Масспектрите са кетони пикове, отговарящи на -razryvu молекули кетони, и най-за предпочитане алкиловата група се отцепва. Така масспектри alifatich. метил кетони съдържат Naib. интензивен пик с M / Z 43 (). За метил кетони също характеристика б -razryv мол. йон миграция от Н гр -атома C (peregruppirovochny пик с M / Z 58). Според степента на оксидация на кетони и алдехиди като. отнеме межд. позиция между алкохоли и-тер, който определя тяхната химична по много начини. комуникационни острови. Кетоните се редуцират до вторични алкохоли с метални хидриди. напр. LiAlH4 или NaBH4. водород (Cat -. Ni, Pd), в присъствието izopropavolom алкоксид Al (р-ТА Meerwein - Ponndorfa - Verley). Когато възстановяването кетони като натриев или електрохимично (катодна редукция), оформен пинакол.
При взаимодействието. кетони сливане с Zn и конц. Солна киселина (р-ТА Clemmensen) или с хидразин в алкална среда (р-ТА Kishner - Wolf) група С = О се редуцира до СН2. За разлика от алдехиди. Много кетони са стабилни, когато се съхранява в продължение на действие O2. Кетони съдържащи -metilenovuyu група SeO2 окислява до 1,2-дикетони по-енергични оксиданти. напр. KMnO4 - до смес от карбоксилна т (виж Popov правило.). Циклична. кетони в взаимодействието. с KMnO4 или HNO3 изложени оксид. разделяне цикъл, например. циклохексанон оформен да адипинова-та. Линейни перкиселини са окислени до кетони естери. циклични - до лактони (р-ТА Bayer - Villiger). За EtOH съдържащ Н-атом, са СН-средно силни киселини (рКа 10-20). Те се характеризират с преобразуваната. в еноли или енолатни аниони.
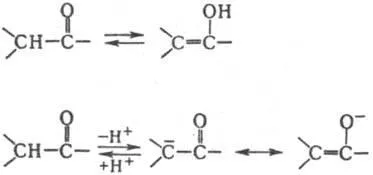
Това се базира на способността на такива кетони реагират като С или О-нуклеофили. Концентрация енолните форми зависи от структурата на кетони и количества (в%): 0.0025 (ацетон), 2 (циклохексанон) 80 (ацетилацетон). Катализирана енолизация до трето и основи. Кетони продукти заместване образуват Н атоми в Br2 действието на халогениране. N-бромосукцинимид, SO2 Cl2. когато tiilirovanii дисулфид. Алкилирането и ацилирането на кетони образува енолати или продукт заместване Н атоми в кетони, О-производни или еноли. От голямо значение в орг. синтез и кротонова имат алдолна кондензация. напр.
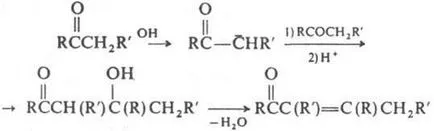
Кондензация на алдехиди с кетони реагират гл. Пр. като СН-киселина, например. от кетони и СН2 О в присъствието. база, получена а, Ь-ненаситен кетони: RCOCH3 + СН2 О. RCOCH = СН2 + H2O Поради полярността на карбонилни групи кетони може да влезе в р-ТА като С-електрофили напр. производни чрез кондензиране с карбоксилна-тон (Stobbe кондензация Darzana р-ТА и др ....):
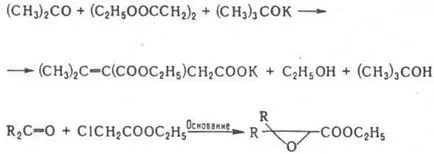
Особено лесно нуклеофил. изложени на нападение а, Ь -nepredelnye кетони, но в този случай двойната връзка е атакуван (р-ТА Michael), например.
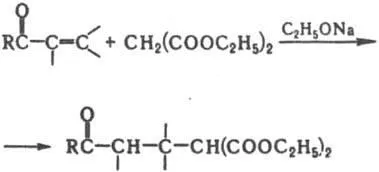
При взаимодействието. илиди с Р (alkilidenfosforanami) кетони обмен О атом в алкилиденова група (р-ТА Wittig): R2 С = О + Ph3 P = CHR '. R2 С = CHR '+ Ph3 PO С циклопентадиенови форма fulveny кетони, напр.
Кондензацията на кетони с хидроксиламин получава ketoximes R2 C = NOH, с хидразин - хидразони R2 C = N- -NH2 азини и R2 C = N-N = CR2. с първични амини - Шифови бази R2 C = NR ', с вторични амини - енамини. Кетони могат да бъдат прикрепени към карбонилната група на вода. алкохоли. бисулфит, натриев, амини и други. нуклеофили, въпреки че р-нето не се срещат като лесно, както в случая на алдехиди. Тъй като алкохол р-ма равновесие между кетона и хемикетал силно измества наляво за получаване на кетали от кетони и алкохоли трудно: RCOR '+ R. ОН D RR'C (OH) OR. За тази цел, р-ТА на кетони с орто-мравчена естери до-ви. Кетони взаимодействие. С-нуклеофили, например. с литий, цинк или magniyorg. Кон. както и с ацетилени в присъствие. основи (р-ТА Tabor), за да образуват третични алкохоли.
Предварително зададените. основи до кетони присъединява HCN, давайки -gidroksinitrily (цианохидрини): R2 С = О + HCN. R2 C (OH) CN С катализа до трето кетони реагират като С-ароматни съединения с електрофили. Кон. напр.
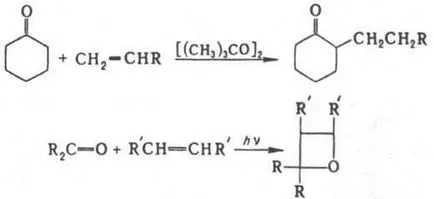
Gomolitich. присъединяване кетони до олефини води до алкил-заместени кетони, fototsikloprisoedinenie да оксетанил. напр.
С Итън играе важна роля в метаболизма на В-В живите организми. По този начин, убихинон участва в оксиди. - възстановяване. р-ции на тъкан дишане. Чрез Кънектикът. съдържащи кетон група са някои важни монозахариди (D-фруктоза и т.н.), терпени (ментон. карвон), основни компоненти на петрола (камфор. jasmone), на стр. багрила (индиго. ализарин. флавони), стероидни хормони (кортизон. прогестерон). Обща Ind. Методи за синтез ketonov- katalitich. окисляване насит. въглеводороди и олефини с кислород. и дехидрогенирането и оксиди. дехидриране на вторични алкохоли. Кетони се синтезират като оксиди. разцепване на 1,2-гликол третичен действие на Pb (OCOCH 3) 4 или NIO4. пиролиза на Са или Ва соли на карбоксилна к-т, преминаване на парите над к-т Co или оксиди на Th, взаимодействието. zfirov или ортоестери на карбонови к-м и ацилхалогениди с Гринярови реагенти или kadmiyorg. Кон. ацилиране аромат преподават. Кон. (Р-ЛИЗАЦИЯ Friedel-Crafts реакция), хидролизиране гем дихалогениди и др. След това ЕЮН се използва като р-erator, екстрагенти за синтеза на полимери. пестициди. стабилизатори. фотографии. лек. и парфюм в и др. Виж. и ацетон. Ацетофенон. Бензофенон. Метил изобутил кетон. Метил етил кетон. Циклохексанонът и др. На специфичност. комуникационни острови дикетони см. дикарбонилни съединения. Литература Бюлер Pearson D. органичния синтез. на. от английски език. Н2, М "1973 .; Общо органичната химия. на. от английски език. Vol. 2, М. 1982, стр. 570-692, 765-847; Химията на карбонилната група, о. 1, изд. от S. Patai, L. N. Y. Сидни, 1966; пак там, кн. 2, изд от J. Zabicky, L, 1970; Houben Weyl, Methoden в органичната Chemie, Bd 7 / 2а, 2Ь, 2с кетон (TI 1 от 3), 4, Aufl, Stuttg. 1973 77. MG Виноградов.
===
App. Литература за тази статия «кетони." неизвестен
