Термично отопление и охлаждане криви метали
Алотропна трансформации в метали.
Тема 1. Структура и кристализация на метали.
2. Кристална структура на металите. Видовете кристални решетки.
1. голям брой различни метали, кото-ръж използвани в областта, могат да бъдат разделени в черно оцветен.
Черни метали са тъмно сиво, с висока плътност, с висока точка на топене, но по отношение на висока твърдост, и в много случаи са по полиморфизъм.
Цветни метали са червено, жълто, бяло оцветяване; имат висока еластичност, ниска твърдост, относително ниска точка на топене; защото те страдат от липса на полиморфизъм-Vie.
За цветни метали включва желязо и неговите сплави, за да цвят - всички други метали и техните сплави.
В зависимост съдържа въглеродни черно-Zhaniya сплави разделени на стомана и чугун.
Това става известен като сплави от желязо с въглерод, в която въглеродният съдържа до 2,14%, и желязо - повече от 2,14%.
Цветни метали са разделени на тежката (мед, олово, калай, никел, и т.н.), лек (алуминий, магнезий и т.н.), редки (молибден, волфрам, ванадий, и т.н.) и скъпоценни (злато, платина, сребро).
2. Всички органи са съставени от атоми. Тяло, кото-ryh атоми са подредени на случаен принцип, се наричат аморфен-ЛИЗАЦИЯ (стъкло, смола, восък, смола, и т.н.). Кристал кал тяло (всички метали и метални сплави tallic), характеризиращ се с раз подредени атомните позиции. В метали и метални SPLA острови атоми са разположени на възлите на пространствено-кристално кристални решетки.
В процеса на кристализация на метали и сплави може да се образува кристална решетка на различни видове. Най-разпространени са тялото центрирана кубична (К, V, Cr, Fe # 945. Mo, W), лице центрирана кубична (Al, Fe # 947. Ni, Cu, Ag, Au, Pb) и шестоъгълна решетка (BE, Mg, Co, Zn, Ti). Лице центрирана кубична решетка и шестоъгълна близкото опаковане характеризиращ атоми и компактен тяхното разположение (Фигура 1).
Разстоянията между съседни атоми в кристалната решетка (решетка параметър) е изключително малка. За измерване ги използват специално звено - ангстрьома (А °), което RA-венозна 1А -8 ° = 10 cm, или Nanomet зададена (1 пМ = 10-9 cm).
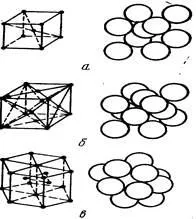
Фиг. 1. подреждането на атомите в решетка-метален Крис:
и - тяло центрирана кубична; б - лице центрирана кубична; в - шестоъгълна
10 Октомври Pa въглерод в графитна форма прекристализира в диамант.
Алотропна форма-полагане на грижи за значителни букви от гръцката азбука: алфа, бета, гама и др ...
За метали не претърпяват алотропна трансформации в твърдо състояние чрез нагряване и охлаждане включват алуминий, магнезий, мед и други. Голям брой технически важни метали (калай, цинк, никел, кобалт и др) открити промени allotropiche небе.
4.Kristallizatsiey наречен образуване на кристали на метали и сплави при преминаване от течност към твърдо вещество (първичен кристализация) и прекристализация в твърдо състояние (средно кристализация).
процес Pro-кристализация на металния елемент се състои от две Търи процеси: зародиши (зародиши) и кристален растеж от тези центрове. Когато температурата на кристализация в стопения метал се образуват първите кристализационни центрове, и тяхната роля играят различни примеси малката шлака и неметални включвания. След образуването на нуклеиращи мехурчета е течен метал атома, разположени bespo-ryadochno започват да се увеличи около тези шийки и източник-форма кристали с правилна геометрична форма. Тъй като едновременно кристализация започва, но на много места и растеж на кристал е във всички посоки, съседните кристали, пред интер-ред, предотвратяване свободен растеж на всеки. Това е, когато води до факта, че кристалите стават неправилна външна форма, независимо от реда им вътре-това е изграждане. Кристалите с неправилна форма, наречени кристалити, polyhedra, или зърна. Получените кристали имат реално някои недостатъци (дефекти) Кристал-кристална структура, която обикновено се класифицират от естеството на тяхната измерване пространство до точката (нула двумерен), линеен (едномерен), повърхността (двумерен), обемен (триизмерна).
Най-често срещаният точка. Те включват позиции (възли кри-кристална решетка, свободен от атоми) междинните атоми (атома в възли е кристална решетка XYZ), както и на онечиствания атоми. (Фигура 2).
Фиг. 2. Точка дефекти в кристалната решетка:
и - вакантно; б - интерстициален атом; в - въвеждане на примес атом
5. При спазване на обратимо топлинно нето на чист метал могат да бъдат построени криви ОХ-охлади нагряването и координира температура - време. Съответно хоризонтален участък и температура крива съществува-стоп - температура Harden-vanija или топене на чист метал.
Тъй абсорбция метал топене латентна топлина температура остава постоянно (т.т.), който е маркиран върху хоризонтална крива графика част отопление (Фиг. 3a). Едва след металните раси стопи напълно, температурата се повишава по наклонената част на кривата.
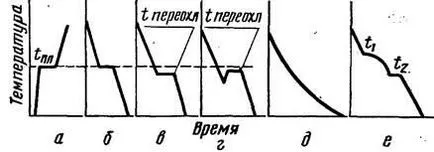
Фиг. 3. Кривите на загряване и охлаждане на чист метал крак тяло аморфен сплав и:
и - крива отопление; б - охлаждане крива без преохлаждане; в - кривата с хипотермия; R - крива с контур Недогряване на водата; г - охлаждане крива на аморфно твърдо вещество; д - охлаждащата крива на сплавта