Как да се намери броя на протоните и неутроните правят всичко себе си
Протоните и неутроните се съдържат в ядрената ядрото, се наричат нуклоните. От факта, че действителната маса на всеки атом се концентрира в основата си, за масовото число на атома е броят на нуклоните. С помощта на периодичната таблица на химичните елементи е разрешено да се установи броят на протоните и неутроните. Той също така могат да се използват и други методи.
- - периодичната таблица на химичните елементи;
- - таксата за протон;
- - индикации за химични елементи.
инструкция
1. Всяка атом съответства вещество елемент от периодичната таблица. Откриване на елемент за брой атом в ядрото на протони и неутрони, които трябва да се открие. Определяне на ядрената количество на елемента. Той се намира в долната част на клетката, която се намира химичен елемент. Ако масовото число е представена от частична стойност, тя се закръгля до най-близкото цяло. Този брой е равен на броя на нуклоните в атома. Например, магнезиев определи ядрена маса. Откриване на активния елемент в периодичната таблица, има обозначение Mg. Нейната маса номер е 24.305. Кръгла това до цялото и се 24. Това означава, че броят на протоните и неутроните (нуклоните) в ядрото на атом на елемента е 24.
2. Определяне на броя на протоните в ядрото на атом. За това, че се открие в периодичната таблица на химичните елементи. В горната част на член забелязани от неговия сериен номер в един ред в клетка от таблицата. Това е броят на протоните в ядрото на атом елемент. Например, номер на последователност на магнезий (Mg) е равен на 12. Това означава, че 12 протони, които се съдържат в ядрото.
3. От време на време да се ограничи до ядрен заряд в кулони, а след това, за да се открият броя на протоните, разделете това число от таксата на един протон, който е равен на 1,6022 • 10 ^ -19 Кулон. Например, ако на известния заряд на ядрото на 35.2 • 10 ^ -19 Кулон, а след това да го разделя от 1,6022 • 10 ^ -19 получите номера. приблизително равна на 22. Това означава, че в ядрото на атома 2 протона.
4. По-късно определяне на броя на протоните откриване броя на неутроните в ядрото. За тази относителното тегло на ядрото на ядрен открити с помощта на периодичната таблица на химичните елементи, изваждане на броя на протоните, съдържащи се в ядрото. От факта, че в допълнение към неутронните други тежки частици в ядрото на атом не се съдържа, ще бъде броя на неутроните. Например, ако е необходимо да се установи броят на протоните и неутроните в ядрото на фосфор (Р) го открие в периодичната таблица, определяне на броя на маса и серийния номер на елемента. Масовият броя на фосфор е равна 30.97376? 31 и серийния номер 15. Това означава, че ядрото на атом на химичния елемент съдържа 15 протона и 16 неутрони = 31-15.
Atom химичен елемент се състои от ядрено ядро и електрони. Съставът на ядрената ядрото включва два вида частици - протони и неутрони. Приблизително една атомна маса е концентрирана в сърцевината, поради протоните и неутроните са много по-тежки от електрони.

- атомен номер, изотопи
инструкция
1. За разлика от протоните, неутроните нямат електричен заряд, т.е. тяхната електрически заряд е нула. Следователно, знаейки, броят на основните елементи, не е възможно да се каже със сигурност колко неутрони, които се съдържат в ядрото му. Например в ядро въглеродни атоми неизменно съдържа 6 протони, протони въпреки че могат да бъдат 6 и 7. Вариации ядра химичен елемент с различен брой неутрони в ядрото се наричат изотопи на този елемент. Изотопи могат да бъдат естествени и неестествени получен.
2. Ядрена ядро определен азбучен символ на химичен елемент от периодичната таблица. В дясно на символа в горната и в долната част има две числа. Горният номер - е масовото число на атома, А = Z + N, където Z - ядрен заряд (брой протони), и N - chisloneytronov. Долната броя - е най-Z - отговаря за ядрото. Този запис съдържа информация за броя на неутроните в ядрата. Очевидно е, че е равен на N = A-Z.
3. различни изотопи на химичен елемент редица промени, което се отразява в записа на този изотоп. Някои изотопи са истинските им имена. Например, обикновено водород ядро не разполага с неутрони и протон. Водородни изотопи деутерий е един неутрони (А = 2) и тритий изотоп - две неутрони (А = 3).
4. Свързаност брой неутрони, записани от броя на протоните в N-Z диаграма ядрени ядра. Стабилността на ядра зависи от съотношението на броя на неутроните и броя на протоните. Сърцевини леки нуклиди особено стабилна, когато N / Z = 1, т.е., с равен брой неутрони и протони. С увеличаване на броя на масови смени област стабилност на стойностите на N / Z> 1, достигайки стойност на N / Z
1.5 за особено тежки ядра.
Атомът на химичен елемент се състои от ядро и ядрената електрони обвивка. Съставът на ядрената ядрото включва два вида частици - протони и неутрони. Приблизително една атомна маса е концентрирана в сърцевината, така както протони и неутрони са много по-тежки от електрони.

- Броят атомната елемент, N-Z диаграма.
инструкция
1. неутроните нямат никаква електрически заряд, т.е. тяхната електрически заряд е нула. Това е основната трудност при определяне на броя на неутроните - ядрената номер на елемента или електронния му обвивка не даде ясен резултат по този въпрос. Например, в ядро въглеродни атоми неизменно съдържа 6 протони, протони въпреки че могат да бъдат 6 и 7. Вариации ядра химичен елемент с различен брой неутрони в ядрото се наричат изотопи на този елемент. Изотопи могат да бъдат естествени, или могат да бъдат получени и неестествени.
2. ядрата на атомите означени азбучен символ на химичен елемент от периодичната таблица. В дясно на символа в горната и в долната част има две числа. Горният брой е А - е масовото число на атома. А = Z + N, където Z - ядрен заряд (брой протони), и N - броя на неутроните. Долната броя - е най-Z - отговаря за ядрото. Този запис съдържа информация за броя на неутроните в ядрата. Очевидно е, че е равен на N = A-Z.
3. Различните изотопи на химичен елемент редица промени, които имат право да се видят в записа на този изотоп. Някои изотопи са истинските им имена. Например, обикновено водород ядро не разполага с неутрони и протон. Водородни изотопи деутерий е един неутрони (А = 2, фигура 2 от по-горе, от долу 1), и тритий изотоп - две неутрони (А = 3, фигура 3, по-горе, по-долу 1).
4. свързаност на неутрони от броя на протоните се отразява в така наречените N-Z диаграма ядрени ядра. Стабилността на ядра зависи от съотношението на броя на неутроните и броя на протоните. Сърцевини леки нуклиди особено стабилна, когато N / Z = 1, т.е., с равен брой неутрони и протони. С увеличаване на броя на масови смени област стабилност на стойностите на N / Z> 1, достигайки стойност на N / Z
1.5 за особено тежки ядра.
За да се установи броят на протоните в атома определи позицията си на периодичната таблица. Открийте своя сериен номер в периодичната таблица. Тя ще бъде равен на броя на протоните в ядрото ядрена. Ако ние изучаваме изотопа, погледнете една двойка числа, които описват свойствата, долната брой е равен на броя на протоните. В този случай, ако известния заряда на ядрено ядро, позволи да се знае броя на протоните, като стойността на таксата от един протон.
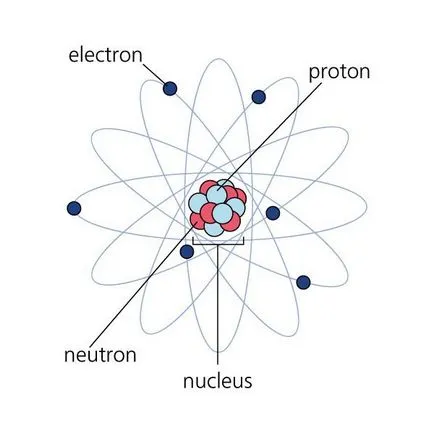
- За да се открият броя на протоните, за да разберете стойността на таксата за протон или електрон, вземете една маса на изотопи, периодичната таблица.
инструкция
1. Определяне на броя на протоните в близост atoma.V когато известният което атом се изучава, да открият местоположението му в периодичната таблица. Идентифицирайте номер в таблицата да се намери клетка на съответния елемент. В клетката откриване на серийния номер на елемента, на който съответства разбере атом. Този сериен номер ще съответства на броя на протоните в ядрената ядрото.
2. Методи за откриване на протоните в izotope.Mnogie изотопи на атоми имат различни маси ядра. Следователно е само масата на ядрото е незадоволителен за недвусмислено определяне на ядреното ядро. При представянето на изотопа, преди да запишете неговото химично наименование, последователно записва двойка числа. Горната число показва масата на атома в атомни единици за маса, а на дъното показва заряда на ядрото. Целият блок, който отговаря за ядро такива записи съответства на един протон. По този начин, броят на протоните, равни на по-малкия брой на записите в даден изотоп.
3. Методи за откриване на протони знае yadra.Zachastuyu събират свойства на ядра атом се характеризира с заряда. За да се определи броя на протоните в него, трябва да го преведе на висулки (ако той е работил в няколко единици). След това разделете на таксата върху основния модул електронен заряд. Това се дължи на факта, че на този атом е електрически неутрален, броя на протоните в него, равен на броя на електрони. И техните такси са равни по сила и противоположни по знак (протон има необходимото за заряда на електрона - отрицателни). Следователно зареждане на разделение на атом ядра на броя 1,6022 • 10 ^ (- 19) медальон. Това ще има броя на протоните. От факта, че методите за измерване на атомната такса задоволително точен в случая, ако разделението се обърна с дробно число, то закръглят към цялото.
Атомите състоят от елементарните частици - протони, неутрони и електрони. Протоните са правилно заредени частици, които са в центъра на атом в ядрото. Изчислява се броят на протоните оставя изотоп ядрената номер на съответния химичен елемент.
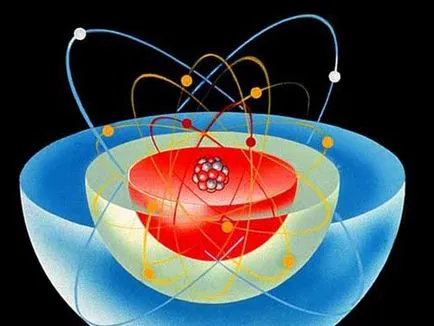
атом модел
За да обясни свойствата на атома и дизайнът му модел се прилага, със сигурност под името "Бор модел на атома". В съответствие с този атом дизайн напомня на ясна система - значително център (ядро) се намира в центъра, и повечето от леки частици се движи в орбита около него. На неутроните и протоните образуват положително заредена ядрото и отрицателно заредени електрони се движат около център, се привлича към него чрез електростатично silami.Elementom наречен вещество, съставено от атоми от един вид, се определя от броя на протоните във всички от тях. Компонент се определя име и символ, например, водород (Н) или кислород (О). химичните свойства на елемент зависят от броя на електрони и съответно броя на протоните, съдържащи се в атомите. Химическа kollyatsii атом не зависи от броя на неутроните, защото неутроните нямат електричен заряд. Въпреки това броят им влияе на стабилността на ядрото променя атомен обща маса.
Изотопи и броя на протоните
Изотопи на атоми, се наричат отделни елементи с различен брой неутрони. Тези атоми са химически същия обаче различни собствено тегло, те също се различават по тяхната способност да излъчват izluchenie.Yaderny номер (Z) - е поредният номер на химичния елемент в периодичната система, се определят от броя на протоните в ядрото. Всички ядрени характеризиращ брой атом и масовото число, (А), който е равен на общия брой на протоните и неутроните в ядрото. Елементът може да има различен брой атоми с неутроните, но броят на протоните остава твърдо и е равен на броя на електроните на неутрален атом. С цел, за да се определи каква част от протони, които се съдържат в ядрото на изотопа, доста да погледнете ядрената си номер. Броят на протоните, равен на броя на съответния химичен елемент в периодичната таблица.
Например, изотопи на водород е позволено да се види. В природата, водородни атоми са особено често срещани с един протон и не неутрони. В същото време, има изотопи на водород с един или два неутрони, те имат съответните препратки. Въпреки това всички те имат един протон, който съответства на поредния номер на водород в периодичната таблица. водороден изотоп с масово число на неутрони и 2 се нарича тежък водород или деутерий, той е стабилен. Тритий е водороден изотоп с масовото число, 3, и двете неутроните, радиоактивни. Неговата понякога се нарича супер тежък водород и тритий ядро - Тритон.
виж също
- Как да се определи коефициентът на триене

- Как да намерите силата на триене при плъзгане

- Как да платя за отпуск за отглеждане на дете до 3 години

- Как да променя кожено палто
