Формула амоняк в Chemistry
Амоняк - е неорганично съединение се от водород и азот със степен на окисление на азот.
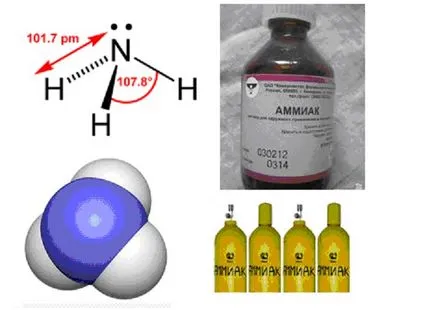
Моларен маса е г / мол.
Физични свойства - амоняк е безцветен газ с остра миризма, точка на топене, точка на кипене, е добре разтворим във вода (при 30 с масова плътност от 0,892 грама / мл), алкохол и редица други органични разтворители.
Химичните свойства на амоняк
- експонати амфотерни свойства (много слаби киселинни свойства) следователно реагират с алкални метали с киселини, с окислители с преход метални йони:
Получаване на амоняк
Промишлено амоняк, получени директно чрез взаимодействие на водород и азот в присъствието на различни катализатори (платина, никел, желязо):
В лабораторията, амонякът произведени чрез действието на силна алкален на амониевата сол чрез нагряване:
приложение
Амонякът се използва за производство на азотни торове, взривни вещества, различни полимери, използвани в производството на азотна киселина, сода и други химически продукти също да намери приложение в медицината като респираторен патоген стимулатор емезис лосиони. Течен амоняк се използва като разтворител.
качествена реакция
Качествена реакция на амоняк се превръща синьо лакмусова хартия, навлажнена с вода. Други качествена реакция на амоняк - е образуването на жълто-кафява утайка при взаимодействие на амоняк с реагент Nessler е:
Примери за решаване на проблеми
Изчислява равновесната константа на реакцията на разтваряне на разтвора на утайка амоняк поради образуване на комплекс.
Пишем уравненията на реакциите:
Пишем реакцията от постоянна маса и изчисли магнитуд:
- разтворимост продукт
- нестабилност постоянна
1 литър газ при нормални условия и съдържащи абсорбира примеси индиферентни мл разтвор с моларност на 1 мол / л. Излишният разтвор се титрува с 20 мл моларност от 0,1 мол / л. Определя обемната фракция на газовата смес.
Пишем уравненията на реакциите:
Ние изчисляваме първоначалния брой молове.
Изчисляват излишък брой молове:
Намерете броя на моловете, която продължи усвояването:
Изчислява се броят на моловете, а обемът:
- моларно обем на идеалния газ при нормални условия.
Ние изчисляваме обемната фракция: