алкани лекция
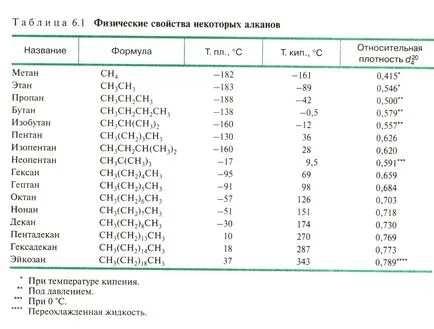
Физични свойства на алкани - виж урока ..
Методи за получаване на алкани
Източници на промишленото производство на алкани - природен газ, нефт.
Синтетични методи (използват главно в лабораторията за получаване на комплексни алкани):
1. хидрогениране на алкени и алкини
2. Възстановяване на халоалкани
4. Реакционната Wurtz
5. Колбе реакция
Химическа реакция - обикновено е многоетапен процес. Тя започва с разчупването на връзки в изходните съединения, последвано от образуването на нови връзки и нови връзки. По време на реакцията, нестабилни междинни продукти се образуват частици. Последователността на етапите на механизма за реакция се нарича.
Активната частица - частица, имаща висока химическа активност, те иницииране на реакцията.
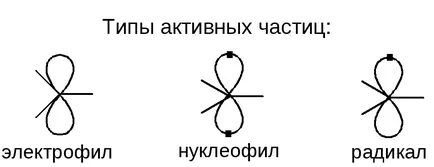
Електрофил - атаки електрон-частици в повишена пространство електронна плътност.
Нуклеофил - ЕЛЕКТРОННИ атаки на частиците в местата за намалена плътност на електрони.
Радикална - електрически неутрални частици, атакува неполярен и малко полярен връзка.
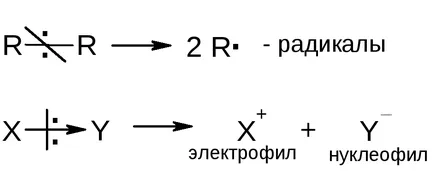
Активните частици могат да бъдат образувани чрез счупване на химичната връзка. Homolytically ниски полярни връзки се разграждат и се образуват два радикала; полярни връзки се разграждат heterolytically и формира нуклеофил и електрофил:
Химичните свойства на алкани
Алкани - най химически инертно вещество.
С-С връзка и С-Н ниска полярност и устойчиви на атаката на електрофили и нуклеофили, те пробие под действието на радикали.
Реакционната механизъм - верига радикал, който:
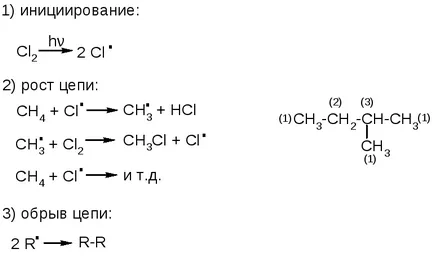
Скоростта на реакцията на първични, вторични и третични въглеродни атоми е различна: увеличава в реда: С (1) <С(2) <С(3) (см. предыдущую схему).
Освен хлориране малко селективно в това отношение, по-селективно бромиране на малка Br радикал активност.
в парна фаза при 400-500 °;
течна фаза - при около 110-140 (Konovalov)
Алкани - един от най-трудните окислени вещества. При стайна температура, те дори не са силни окислители.
В горивната алкани са превърнати до СО2 и Н2 О.
Контролирано окисление на кислород при около 200 и 90 атм. постъпления в течната фаза с разцепване С-С връзки и образуването на смес от карбоксилни киселини.
Например, промишлен метод за получаване на оцетна киселина:
3. Термично разделяне и напукване:
Крекинг е много широко използван в петролев рафиниране за високо октаново гориво.
Някои представители на алканите - виж урока ..
Циклоалкани - наситени въглеводороди с затворена верига.
Общата формула - Cn H2N (моноциклични незаместен).
Те се различават по циклоалкани:
- метод за съединяване на цикъла.
Моноцикличен. циклопропан, циклобутан, циклопентан, циклохексан
(Формула обяснява).
а) кондензирани (анелиран):
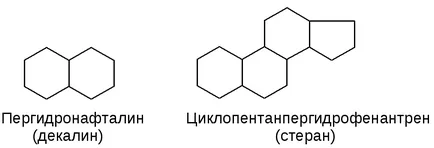


Теория на напрежения (Bayer)
Отклонението на геометричната ъгъл от ъгъла на връзка от 109 произвежда напрежение в цикъла:
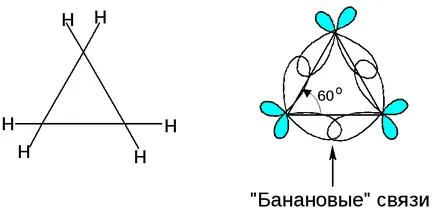
"Банан" комуникация междинен характер между π- и а-връзки: ненаситен циклопропан - свързване реакция цикъл с прекъсване.
Методи за получаване на циклоалкани
1. дехидрогениране дихлороалкани (вариант Wurtz реакция):
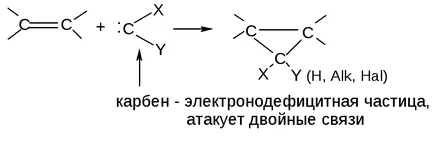
3. синтез диен (Diels-Alder реакция):
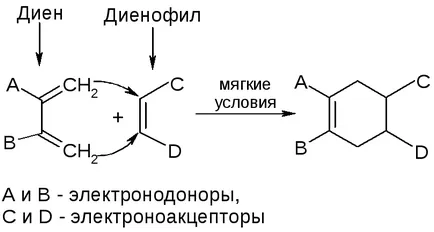
Химичните свойства на циклоалкани
1. Реакции малки цикли:
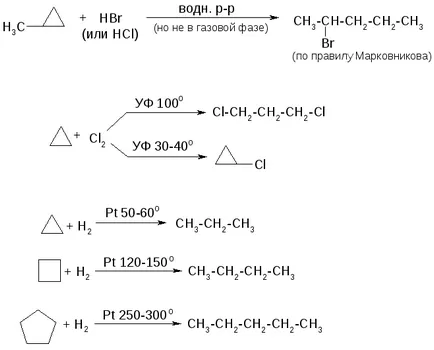
2. реакции в цикъла са почти същите като за ациклени алкани.
Някои представители на цикло - виж урока ..